Пандемия коронавируса и то, как мир боролся с ней, вызвали к дискуссии много вопросов. Специалисты говорят о новой глобальной биологической войне. В рамках этой дискуссии предлагаем перевод статьи, подписанной несколькими десятками ученых, в которой специалисты поднимают тему опасности вакцин и вакцинации.
Статья сначала была опубликована 8 мая в виде препринта на нескольких языках в консервативных изданиях enVolve (США), FranceSoir (Франция) и других, а затем 18 мая появилась в виде препринта на ресурсе authorea.com. Изначально ее подписали 57 ученых и врачей, из-за чего она и получила расхожее название «доклад 57-ми». В последней версии от 18 мая в списке подписантов указано 50 человек. Позднее, 24 мая, на том же сайте та же статья была опубликована еще раз с незначительными редакционными правками, текст статьи и список подписавших остались неизменными.
Массовая вакцинация от SARS-CoV-2: насущные вопросы о безопасности вакцин, которые требуют ответа от международных здравоохранительных организаций, регулирующих организаций, правительств и разработчиков вакцин
Roxana Bruno, Peter A Mccullough, Teresa Forcades I Vila, et al. SARS-CoV-2 mass vaccination: Urgent questions on vaccine safety that demand answers from international health agencies, regulatory authorities, governments and vaccine developers
Аннотация
С начала вспышки COVID-19 стартовала безудержная и беспрецедентная гонка в тестировании новых платформ, обеспечивающих иммунизацию от SARS-CoV-2, которая привела к экстренному одобрению различных вакцин. Несмотря на ранний прогресс в мультилекарственной терапии для пациентов с COVID-19, действующая в настоящее время установка состоит в максимально быстрой иммунизации населения всего мира.
Отсутствие тщательного тестирования на животных перед клиническими испытаниями и выдача разрешений на основании данных о безопасности, собранных во время испытаний длительностью менее 3,5 месяцев, поднимают вопросы о безопасности этих вакцин.
Недавно определенная роль спайк-гликопротеина, вызывающего повреждения эндотелия, характерные для COVID-19, даже в отсутствие заражения, исключительно важна, поскольку большинство одобренных вакцин вызывают выработку спайк-гликопротеина у вакцинированных.
Учитывая большую частоту возникновения побочных эффектов и большое разнообразие обнаруженных к настоящему моменту типов побочных эффектов, а также потенциал для усиления заболевания под действием вакцины, Th2-иммунопатологию, аутоиммунные реакции и иммунную эвазию (уклонение от распознавания иммунной системой), необходимо лучше понять выгоды и риски массовой вакцинации, особенно в группах, которые не участвовали в клинических испытаниях.
Несмотря на призывы к осторожности, риски вакцинации от SARS-CoV-2 занижаются или игнорируются здравоохранительными организациями и правительственными учреждениями.
Как и для любой экспериментальной биомедицинской программы, советы по мониторингу данных безопасности (DSMB) и комиссии по экспертной оценке явлений (EAC) должны предписывать уменьшение рисков. Если DSMB и EAC этого не делают, мы призовем к приостановке массовой вакцинации. Если DSMB и EAC не существуют, то вакцинация должна быть немедленно остановлена, особенно для демографических групп с максимальным риском смерти, связанной с вакцинацией, или серьезных побочных эффектов.
Мы настаиваем на необходимости широкого диалога в контексте политики здравоохранения, выделяя критические вопросы, требующие срочных ответов, если мы хотим избежать глобального разрушения доверия к науке и народному здравоохранению.
Введение
После того как в марте 2020 года была объявлена пандемия COVID-19, по всему миру сообщили о более 150 миллионов случаев заражения и 3 миллионах смертей. Несмотря на прогресс в ранней амбулаторной мультилекарственной терапии для пациентов с высоким риском, который привел к сокращению на 85% числа госпитализаций с COVID-19 и смертей[1], принятая в настоящее время установка состоит в массовой вакцинации.
Хотя мы отдаем должное усилиям по разработке, производству и экстренному одобрению вакцин от SARS-CoV-2, мы озабочены тем, что здравоохранительными организациями и правительственными учреждениями риски занижаются или игнорируются, несмотря на призывы к осторожности[2-8].
Вакцины для других коронавирусов никогда не одобряли для людей, и данные, полученные в ходе разработки вакцин от коронавирусов, призванных вырабатывать нейтрализующие антитела, показывают, что они могут утяжелить заболевание COVID-19 из-за антителозависимого усиления (ADE) или Th2-иммунопатологии, независимо от платформы, на которой разработана вакцина и от метода доставки[9-11].
Известны случаи усиления заболевания у животных, привитых от SARS-CoV и MERS-CoV, их приписывают иммунным комплексам и поглощению вируса макрофагами под действием Fc-рецепторов, что усиливает активацию T-клеток и воспаление[11-13].
В марте 2020 иммунологи и эксперты по коронавирусам оценили риски вакцин от SARS-CoV-2, основываясь на испытаниях вакцин от SARS-CoV, проведенных на модельных животных.
Группа экспертов заключила, что ADE и иммунопатология являются реальной угрозой, но решили, что их риск недостаточен для того, чтобы отложить клинические испытания, хотя необходимо вести постоянное наблюдение [14]. Хотя у добровольцев, привитых вакцинами от SARS-CoV-2, не было зарегистрировано явных симптомов ADE и вызванной вакцинами иммунопатологии, в ходе испытаний на безопасность эти серьезные негативные последствия (SAE) не исследовались.
Поскольку длительность наблюдения за добровольцами не превышала 3-3,5 месяцев после получения второй дозы [16-19], обнаружение SAE маловероятно.
Несмотря на ошибки в отчетах, невозможно игнорировать тот факт, что даже после того, как были сделаны миллионы прививок, по данным американской системы оповещения о негативных последствиях вакцинации (VAERS), число смертей на миллион введенных доз вакцины увеличилось более, чем в 10 раз. Мы убеждены в необходимости открытого научного диалога по вопросу безопасности вакцин в контексте масштабной иммунизации.
В данной работе мы описываем некоторые из рисков массовой вакцинации в контексте критериев исключения из третьей фазы испытаний и обсуждаем SAE, о которых сообщали национальные и региональные системы регистрации негативных последствий. Мы отмечаем вопросы, которые остались без ответов и привлекаем внимание к необходимости более осторожного подхода к вакцинации.
Критерии исключений для третьей фазы испытаний вакцины от SARS-CoV-2
С некоторыми исключениями, в третьей фазе испытаний вакцины от SARS-CoV-2 не участвовали люди старшего возраста, что сделало невозможным определить распространенность эозинофильного лейкоцитоза и усиления воспаления после вакцинации у людей старшего возраста.
Изучение вакцин от SARS-CoV показали, что у иммунизированных мышей старшего возраста был особенно высокий риск опасной для жизни Th2-иммунопатологии [9,20]. Несмотря на эти симптомы, а также на исключительно ограниченные данные о безопасности и эффективности вакцин от SARS-CoV-2 для людей старшего возраста, кампании по массовой вакцинации с самого начала сфокусировались на этой возрастной группе.
Также большинство испытаний исключало беременных и кормящих добровольцев, лиц с такими хроническими заболеваниями, как туберкулез, гепатит С, аутоиммунная реакция, коагулопатия (нарушение свертываемости крови), рак, иммуносупрессия (подавление иммунитета) [16-29], хотя теперь данным категориям предлагают вакцинироваться, предполагая безопасность.
Еще один критерий исключения почти для всех испытаний — контакт с SARS-CoV-2 до вакцинации. Это очень неудачно, поскольку не дало возможности получить исключительно нужную информацию о случаях пост-вакцинального ADE у людей, которые уже имеют антитела к SARS-CoV-2.
Насколько мы знаем, за ADE нет систематического наблюдения ни для одной группы вакцинированных, отобранной по возрасту или медицинским показаниям. Более того, несмотря на существенную долю тех, кто уже имеет антитела [21], тестирование на антитела SARS-CoV-2 перед вакцинацией не сделано обязательным.
Останутся ли незамеченными серьезные негативные последствия вакцин от SARS-CoV-2?
COVID-19 включает в себя широкий спектр клинических симптомов, от легких до тяжелых форм легочной патологии и фатальных случаев с поражением нескольких органов, воспалений, нарушений работы сердечно-сосудистой системы, дисрегуляции свертываемости крови [22-24].
В этих случаях проявления вызванного вакциной ADE или иммунопатологии будут клинически неотличимы от тяжелой формы COVID-19 [25].
Более того, даже в отсутствие вируса SARS-CoV-2, спайк-гликопротеин сам по себе вызывал повреждение эндотелия и повышение кровяного давления как в лабораторных условиях, так и в опытах на сирийских хорьках, подавляя ангиотензинпревращающий фермент 2 (ACE 2) и нарушая работу митохондрий [26].
[эндотелий — важнейший элемент стенок кровеносных сосудов, состоящий из плоских клеток, однослойный полупроницаемый пласт между кровью и тканями. Он выполняет множество функций и участвует в различных физиологических процессах. В частности, эндотелий регулирует питание, препятствует адгезии тромбоцитов, обладает антигенной активностью и способностью к фагоцитозу, участвует в управлении свертываемостью крови и защите от воспалений. Повреждение эндотелия может приводить к нарушениям в работе этих механизмов, в частности — к образованию атеросклеротических бляшек и тромбозу — ИА Красная Весна]
Хотя эти данные еще не подтверждены на людях, возможные их последствия сокрушительны, поскольку все вакцины, одобренные для экстренного применения, основаны на введении или выработке спайк-гликопротеина.
Для вакцин, основанных на мРНК или на аденовирусном векторе, нет ни единого исследования, где проверялась бы длительность синтеза спайк-гликопротеина в организме после вакцинации. Исходя из принципа осторожности, следует предполагать, что вызванная вакцинацией выработка спайк-гликопротеина может вызывать клинические признаки тяжелой формы COVID-19 и может быть ошибочно принята за случай нового заражения SARS-CoV-2.
Поэтому истинные последствия нынешней глобальной стратегии вакцинации могут остаться нераспознанными, если не проводить специальных исследований этого вопроса.
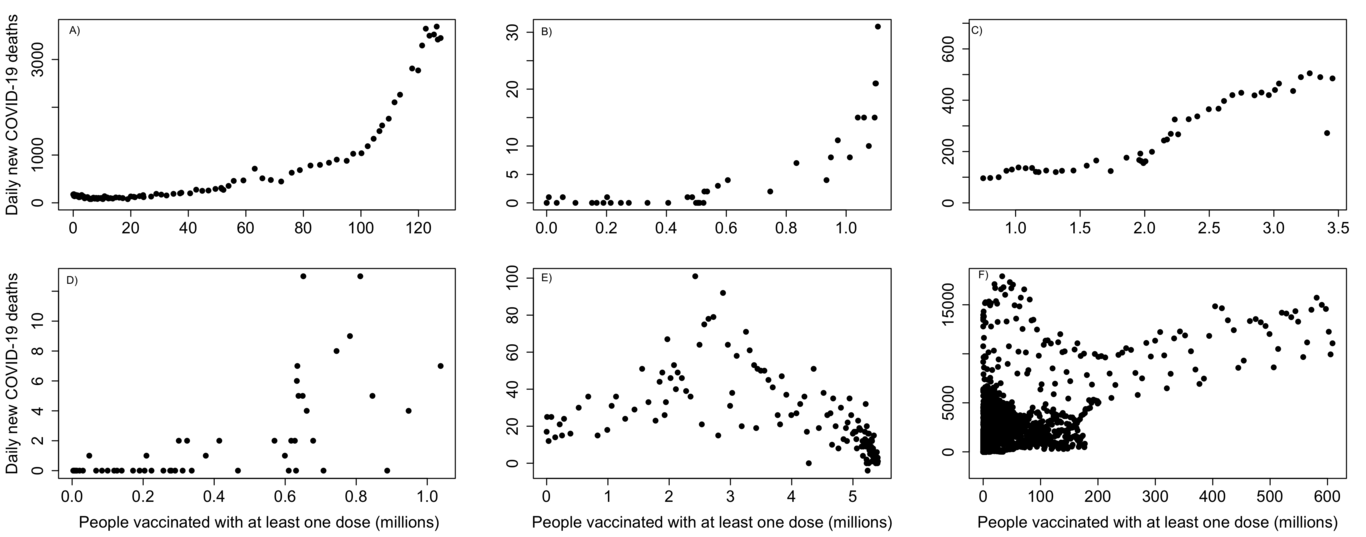
Уже есть необъясненные свидетельства о временном или постоянном увеличении смертности от COVID-19 после вакцинации в некоторых странах (Рис.1), и в свете патогенности спайк-гликопротеина, эти смерти требуют глубокого изучения, чтобы определить их отношение к вакцинации.
Непредвиденные побочные реакции на вакцины от SARS-CoV-2
Еще один важный вопрос требует ответа из-за глобального масштаба вакцинации от SARS-CoV-2 — аутоиммунные реакции. SARS-CoV-2 имеет множество иммуногенных протеинов, и все, кроме одного, иммуногенные эпитопы имеют сходство с человеческими протеинами [27].
Они могут стать источниками антигенов, вызывающими аутоиммунные реакции [28]. Хотя тот же эффект может проявиться при инфицировании натуральным SARS-CoV-2, вакцинация предназначена для большинства человечества.
В то же время, по оценкам исполнительного директора Программы по чрезвычайным ситуациям в области здравоохранения Всемирной организации здравоохранения доктора Майкла Райана, вирусом SARS-CoV-2 заразились лишь 10% населения Земли. Мы не смогли найти свидетельств о том, что какая-то из одобренных вакцин исследована на наличие таких эпитопов, чтобы исключить потенциальную возможность аутоиммунных реакций из-за патогенного примирования (первичной иммунизации).
Часть побочных реакций, включая нарушения свертываемости крови, уже наблюдалась после вакцинации здоровых молодых людей. Эти случаи приводили к приостановке или прекращению использования аденовирусных векторных вакцин ChAdOx1-nCov-19 и Janssen в некоторых странах.
Предполагается, что вакцинация ChAdOx1-nCov-19 может приводить к иммунной тромбоцитопении (VITT), опосредованной антителами к PF4, активирующими тромбы, которая клинически имитирует тромбоцитопению, вызванную гепарином [29].
К сожалению, при одобрении вакцин этот риск был оставлен без внимания, хотя тромбоцитопения, вызываемая аденовирусами, известна уже более 10 лет и является прогнозируемым эффектом для аденовирусных векторов [30]. Риск VITT предположительно выше для тех, кто уже имеет повышенный риск тромбоза, включая женщин, принимающих оральные контрацептивы [31], что требует, чтобы врачи предупреждали своих пациентов.
На уровне популяции возможно еще одно влияние вакцин. SARS-CoV-2 — быстро мутирующий РНК-вирус, который произвел уже более 40 000 вариантов [32,33], некоторые из которых затрагивают спайк-гликопротеин [34,35].
С учетом скорости мутации, вызванная вакцинацией генерация большого количества антител к спайк-гликопротеину может привести к неоптимальному ответу вакцинированного человека на новый вариант вируса.
Этот феномен называют антигенным импринтингом или феноменом первичного антигенного греха. Неизвестно, до какой степени мутации, меняющие антигенные свойства SARS-CoV-2, будут сохраняться при эволюции вируса, но вакцины, вероятно, могут помогать в отборе наиболее заразных вариантов.
Учитывая большое сходство между различными вариантами SARS-CoV-2 этот сценарий маловероятен [32,34], но если будущие варианты будут иметь больше различий в ключевых эпитопах, глобальная стратегия вакцинации может помочь в формировании более опасного вируса. Этот риск недавно был предъявлен ВОЗ в открытом письме [40].
Обсуждение
Риски, обозначенные здесь, являются серьезными препятствиями для продолжения глобальной вакцинации от SARS-CoV-2. Прежде чем подвергать все больше людей риску от этих экспериментов, необходимо получить свидетельство безопасности всех вакцин от SARS-CoV-2, поскольку выпуск вакцины-кандидата без полного понимания результата их действия на здоровье может привести к усилению нынешнего глобального кризиса [41].
Необходимо деление вакцинируемых на группы по степени риска. В соответствии с данными правительства Великобритании, люди моложе 60 лет имеют исключительно низкий риск смерти от COVID-19 [а]. Однако, по данным европейского медицинского агентства Eudravigillance, большинство серьезных побочных эффектов после вакцинации от SARS-CoV-2 зафиксировано у людей в возрасте от 18 до 64 лет.
Особенно беспокоит план вакцинации детей от 6 лет в США и Великобритании. Доктор Энтони Фаучи недавно объявил, что тинэйджеры по всей стране будут вакцинированы осенью, а те, кто младше — в начале 2022 года.
В Великобритании ожидают результатов испытаний, чтобы начать вакцинацию 11 миллионов детей до 18 лет. Для вакцинации здоровых детей нет научного обоснования, поскольку по данным Центров по контролю и профилактике заболеваний США в случае заражения SARS-CoV-2 выживают 99,997% детей.
Мало того, что для этой группы SARS-CoV-2 не является угрозой, еще нет достоверных данных, подтверждающих эффективность вакцины для этой группы и гарантирующих отсутствие опасных побочных эффектов этих экспериментальных вакцин. Поэтому, когда доктор рекомендует пациенту пройти вакцинацию, требуется лучшее понимание выгод и рисков от вакцинирования, особенно в неизученных группах.
В заключение, в контексте поспешного экстренного одобрения вакцин от SARS-CoV-2 и нынешних пробелов в нашем понимании их безопасности, нужно поднять следующие вопросы:
Известно ли, как перекрестно-реагирующие антитела от предыдущего контакта с коронавирусом или вызванные вакцинацией могут повлиять на риск опасных побочных эффектов от вакцинации против COVID-19?
Был ли конкретный риск ADE, иммунопатологии, аутоиммунных реакций и опасных побочных реакций ясно предъявлен получателю вакцины, чтобы выполнить условие медицинского этического стандарта, требующего, чтобы пациент понимал, на что он соглашается, давая информированное согласие? Если не был, то по какой причине, и как этого можно добиться?
Как можно обосновать поголовную вакцинацию, если риск умереть от COVID-19 различается в зависимости от возрастной группы и состояния здоровья, а также из третьей фазы испытаний были исключены люди старшего возраста, дети и имеющие различные ограничения?
Каковы права пациента, который получил вред от вакцинации от SARS-CoV-2? Кто будет платить за лечение? Если лечение будет идти за государственный счет, то знает ли общественность о том, что производители вакцин переложили свою ответственность на плечи налогоплательщиков?
В контексте этих опасений, мы предлагаем остановить массовую вакцинацию и открыть неотложный, плюралистический, критический и научно-обоснованный диалог о вакцинации против SARS-CoV-2 среди ученых, медицинских работников, международных здравоохранительных организаций, регулирующих органов, правительств и разработчиков вакцин. Это единственный способ заполнить существующую пропасть между научным доказательством и политикой общественного здравоохранения в отношении вакцин от SARS-CoV-2.
Мы убеждены, что человечество заслуживает более глубокого понимания рисков, чем существует в навязываемой сейчас официальной позиции. Открытый научный диалог незаменим и неотложен для того, чтобы избежать разрушения доверия к науке и народному здравоохранению и обеспечить, чтобы ВОЗ и национальные здравоохранительные органы защищали интересы человечества в ходе идущей пандемии. Необходимо возвращение политики здравоохранения к доказательной медицине, опоре на тщательный анализ актуальных научных данных. Следовать науке — настоятельная необходимость.
Читайте также: Ученые преувеличили риски вакцинации от коронавируса — врач
Заявление о конфликте интересов
Авторы заявляют, что исследование было проведено в отсутствие каких-либо коммерческих или финансовых отношений, которые могли бы расцениваться как конфликт интересов.
Литература
1. McCullough PA, Alexander PE, Armstrong R, et al. Multifaceted highly targeted sequential multidrug treatment of early ambulatory high-risk SARS-CoV-2 infection (COVID-19). Rev Cardiovasc Med (2020) 21:517–530. doi: 10.31083/j.rcm.2020.04.264
2. Arvin AM, Fink K, Schmid MA, et al. A perspective on potential antibody- dependent enhancement of SARS-CoV-2. Nature (2020) 484:353–363. doi: 10.1038/s41586-020-2538-8
3. Coish JM, MacNeil AJ. Out of the frying pan and into the fire? Due diligence warranted for ADE in COVID-19. Microbes Infect (2020) 22(9): 405-406. doi: 10.1016/j.micinf.2020.06.006
4. Eroshenko N, Gill T, Keaveney ML, et al. Implications of antibody-dependent enhancement of infection for SARS-CoV-2 countermeasures. Nature Biotechnol (2020) 38:788–797. doi: 10.1038/s41587-020-0577-1
5. Poland GA. Tortoises, hares, and vaccines: A cautionary note for SARS-CoV-2 vaccine development. Vaccine (2020) 38:4219–4220. doi: 10.1016/j.vaccine.2020.04.073
6. Shibo J. Don’t rush to deploy COVID-19 vaccines and drugs without sufficient safety guarantees. Nature (2000) 579,321. doi: 10.1038/d41586-020-00751-9
7. Munoz FA, Cramer JP, Dekker CL, et al. Vaccine-associated enhanced disease: Case definition and guidelines for data collection, analysis, and presentation of immunization safety data. Vaccine (2021) https://doi.org/10.1016/j.vaccine.2021.01.055
8. Cardozo T, Veazey R. Informed consent disclosure to vaccine trial subjects of risk of COVID-19 vaccines worsening clinical disease. Int J Clin Pract (2020) 28:e13795. doi: 10.1111/ijcp.13795
9. Bolles D, Long K, Adnihothram S, et al. A double-inactivated severe acute respiratory syndrome coronavirus vaccine provides incomplete protection in mice and induces increased eosinophilic proinflammatory pulmonary response upon challenge. J Virol (2001) 85:12201–12215. doi: 10.1128/JVI.06048-11
10. Weingartl H, Czub M, Czub S, et al. Immunization with modified vaccinia virus Ankarabased recombinant vaccine against severe acute respiratory syndrome is associated with enhanced hepatitis in ferrets. J Virol (2004) 78:12672–12676. doi: 10.1128/JVI.78.22.12672-12676.2004
11. Tseng CT, Sbrana E, Iwata-Yoshikawa N, et al. Immunization with SARS coronavirus vaccines leads to pulmonary immunopathology on challenge with the SARS virus. PLoS One (2012) 7(4): e35421. doi: 10.1371/journal.pone.0035421
12. Iwasaki A, Yang Y. The potential danger of suboptimal antibody responses in COVID-19. Nat Rev Immunol (2020) 20:339–341. doi: 10.1038/s41577-020-0321-6
13. Vennema H, de Groot RJ, Harbour DA, et al. Early death after feline infectious peritonitis virus challenge due to recombinant vaccinia virus immunization. J Virol (1990) 64:1407-1409
14. Lambert PH, Ambrosino DM, Andersen SR, et al. Consensus summary report for CEPI/BC March 12-13, 2020 meeting: Assessment of risk of disease enhancement with COVID-19 vaccines. Vaccine (2020) 38(31): 4783-4791. doi: 10.1016/j.vaccine.2020.05.064
15. de Alwis R, Chen S, Gan S, et al. Impact of immune enhancement on Covid-19 polyclonal hyperimmune globulin therapy and vaccine development. EbioMedicine (2020) 55:102768. doi: 10.1016/j.ebiom.2020.102768
16. Folegatti PM, Ewer KJ, Aley PK, et al. Safety and immunogenicity of the ChAdOx1 nCoV-19 vaccine against SARS-CoV-2: a preliminary report of a phase ½, single-blind, randomised controlled trial. Lancet (2020) 396:467–783. doi: 10.1016/S0140-6736(20)31604-4
17. Polack FP, Thomas SJ, Kitchin N. Safety and efficacy of the BNT162b2 mRNA Covid-19 vaccine. N Engl J Med (2020) 383:2603–2615. doi: 10.1056/NEJMoa2034577
18. Ramasamy MN, Minassian AM, Ewer KJ, et al. Safety and immunogenicity of ChAdOx1 nCoV-19 vaccine administered in a prime-boost regimen in young and old adults (COV002): a single-blind, randomised, controlled, phase 2/3 trial. Lancet (2021) 396:1979–93. doi: 10.1016/S0140-6736(20)32466-1
19. Chu L, McPhee R, Huang W, et al. mRNA-1273 Study Group. A preliminary report of a randomized controlled phase 2 trial of the safety and immunogenicity of mRNA-1273 SARS-CoV-2 vaccine. Vaccine (2021) S0264-410X (21)00153-5. doi: 10.1016/j.vaccine.2021.02.007
20. Liu L, Wei Q, Lin Q, et al. Anti-spike IgG causes severe acute lung injury by skewing macrophage responses during acute SARS-CoV infection. JCI Insight (2019) 4(4): e123158. doi: 10.1172/jci.insight.123158.
21. Ioannidis PA. Infection fatality rate of COVID-19 inferred from seroprevalence data. Bull WHO (2021) 99:19–33F. http://dx.doi.org/10.2471/BLT.20.265892
22. Martines RB, Ritter JM, Matkovic E, et al. Pathology and Pathogenesis of SARS-CoV-2 Associated with Fatal Coronavirus Disease, United States Emerg Infect Dis (2020) 26:2005-2015. doi: 10.3201/eid2609.202095
23. Wu Z, McGoogan JM. Characteristics of and Important Lessons From the Coronavirus Disease 2019 (COVID-19) Outbreak in China: Summary of a Report of 72 314 Cases From the Chinese Center for Disease Control and Prevention. JAMA (2020) 323:1239-1242. doi: 10.1001/jama.2020.2648
24. Xu Z, Shi L, Wang Y, et al. Pathological findings of COVID-19 associated with acute respiratory distress syndrome. Lancet Respiratory Med (2020) 8:420-422 doi: 10.1016/S2213-2600(20)30076-X
25. Negro F. Is antibody-dependent enhancement playing a role in COVID-19 pathogenesis? Swiss Medical Weekly (2020) 150:w20249. doi: 10.4414/smw.2020.20249
26. Lei Y, Zhang J, Schiavon CR et al., Spike Protein Impairs Endothelial Function via Downregulation of ACE 2. Circulation Res (2021) 128:1323–1326. https://doi.org/10.1161/CIRCRESAHA.121.318902
27. Lyons-Weiler J. Pathogenic priming likely contributes to serious and critical illness and mortality in COVID-19 via autoimmunity, J Translational Autoimmunity (2020) 3:100051. doi: 10.1016/j.jtauto.2020.100051
28. An H, Park J. Molecular Mimicry Map (3M) of SARS-CoV-2: Prediction of potentially immunopathogenic SARS-CoV-2 epitopes via a novel immunoinformatic approach. bioRxiv [Preprint]. 12 November 2020 [cited 2020 April 19] https://doi.org/10.1101/2020.11.12.344424
29. Greinacher A, Thiele T, Warkentin TE, Weisser K, Kyrle PA, Eichinger S. Thrombotic Thrombocytopenia after ChAdOx1 nCov-19 Vaccination. N Engl J Med (2021). doi: 10.1056/NEJMoa2104840
30. Othman M, Labelle A, Mazzetti I et al. Adenovirus-induced thrombocytopenia: the role of von Willebrand factor and P-selectin in mediating accelerated platelet clearance. Blood (2007) 109:2832–2839. doi: 10.1182/blood-2006-06-032524
31. Ortel TL. Acquired thrombotic risk factors in the critical care setting. Crit Care Med (2010) 38(2 Suppl): S43-50. doi: 10.1097/CCM.0b013e3181c9ccc8
32. Grubaugh ND, Petrone ME, Holmes EC. We shouldn’t worry when a virus mutates during disease outbreaks. Nat Microbiol (2020) 5:529–530. https://doi.org/10.1038/s41564-020-0690-4
33. Greaney AJ, Starr TN, Gilchuk P, et al. Complete Mapping of Mutations to the SARS-CoV-2 Spike Receptor-Binding Domain that Escape Antibody Recognition. Cell Host Microbe (2021) 29:44–57.e9. doi: 10.1016/j.chom.2020.11.007.
34. Lauring AS, Hodcroft EB. Genetic Variants of SARS-CoV-2—What Do They Mean? JAMA (2021) 325:529–531. doi: 10.1001/jama.2020.27124
35. Zhang L, Jackson CB, Mou H, et al. The D614G mutation in the SARS-CoV-2 spike protein reduces S1 shedding and increases infectivity. bioRxiv [Preprint]. June 12 2020 [cited 2021 Apr 19] https://doi.org/10.1101/2020.06.12.148726
36. Korber B, Fischer WM, Gnanakaran S et al. Sheffield COVID-19 Genomics Group. Tracking changes in SARS-CoV-2 spike: evidence that D614G increases infectivity of the COVID-19 virus. Cell (2020) 182:812-827.e19. doi: 10.1016/j.cell.2020.06.043
37. Francis T. On the doctrine of original antigenic sin. Proc Am Philos Soc (1960) 104:572–578.
38. Vibroud C, Epstein SL. First flu is forever. Science (2016) 354:706–707. doi: 10.1126/science.aak9816
39. Weisblum Y, Schmidt F, Zhang F, et al. Escape from neutralizing antibodies by SARS-CoV-2 spike protein variants. Elife (2020) 9:e61312. doi: 10.7554/eLife.61312
40. Vanden Bossche G (March 6, 2021) https://dryburgh.com/wp-content/uploads/2021/03/GeertVandenBosscheOpenLetterWHOMarch62021.pdf
41. Coish JM, MacNeil AJ. Out of the frying pan and into the fire? Due diligence warranted for ADE in COVID-19. Microbes Infect (2020) 22(9): 405-406. doi: 10.1016/j.micinf.2020.06.006
а. Public Health England (PHE) COVID-19 Epidemiology Cell. COVID-19 confirmed deaths in England (to 31 January 2021): report. https://www.gov.uk/government/publications/covid-19-reported-sars-cov-2-deaths-in-england/covid-19-confirmed-deaths-in-england-report
Число умерших от COVID-19 относительно числа людей, вакцинированных хотя бы одной дозой, для каждой из стран. Графики начинаются с 3 марта 2021 года.
Полный список экспертов, подготовивших статью
Roxana Bruno, Peter A. McCullough, Teresa Forcades i Vila, Alexandra Henrion-Caude, Teresa García-Gasca, Galina P. Zaitzeva, Sally Priester, María J. Martínez Albarracín, Alejandro Sousa-Escandon, Fernando López Mirones, Bartomeu Payeras Cifre, Almudena Zaragoza Velilla, Leopoldo M. Borini, Mario Mas, Ramiro Salazar, Edgardo Schinder, Eduardo A. Yahbes, Marcela Witt, Mariana Salmeron, Patricia Fernández, Miriam M. Marchesini, Alberto J. Kajihara, Marisol V. de la Riva, Patricia J. Chimeno, Paola A. Grellet, Matelda Lisdero, Pamela Mas, Abelardo J. Gatica Baudo, Elisabeth Retamoza, Oscar Botta, Chinda C. Brandolino, Javier Sciuto, Mario Cabrera Avivar, Mauricio Castillo, Patricio Villarroel, Emilia P. Poblete Rojas, Bárbara Aguayo, Dan I. Macías Flores, Jose V. Rossell, Julio C. Sarmiento, Victor Andrade-Sotomayor, Wilfredo R. Stokes Baltazar, Virna Cedeño Escobar, Ulises Arrúa, Atilio Farina del Río, Tatiana Campos Esquivel, Patricia Callisperis, María Eugenia Barrientos, Christian Fiala, Karina Acevedo-Whitehouse.